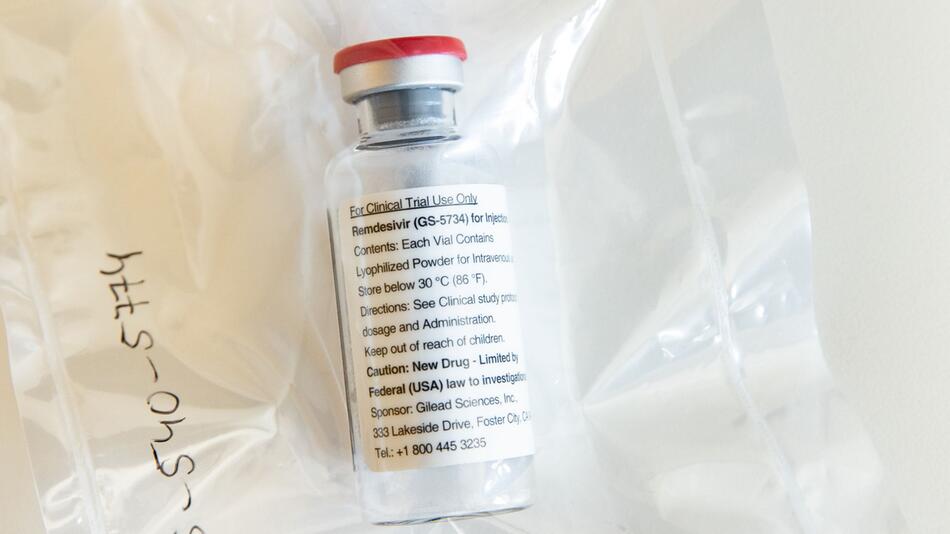
Das Ebola-Medikament Remdesivir gilt schon seit Längerem als das erfolgversprechendste Mittel gegen COVID-19. Nun kamen offenbar US-Forscher, die Remdesivir bei mehr als Hundert schwer kranken Corona-Patienten getestet haben, zu einem bemerkenswerten Ergebnis. Ein wissenschaftlicher Beweis über die Wirksamkeit fehlt aber nach wie vor.
Das Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM) hält die Zulassung eines Medikaments gegen die vom Coronavirus verursachte Lungenerkrankung COVID-19 noch in diesem Jahr für möglich.
Der Wirkstoff Remdesivir gelte dabei als der erfolgversprechendste und sei auch von der WHO empfohlen worden, sagte BfArM-Präsident Karl Broich dem "Bonner General-Anzeiger". Ihm zufolge würden derzeit mehrere klinische Prüfungen zu dem virushemmenden Mittel laufen.
Für ausgewählte Einzelfälle setzen unter anderem schon jetzt die Düsseldorfer Uniklinik und das Hamburger Universitätsklinikum Eppendorf Remdesivir bei COVID-19-Patienten ein – obwohl es noch keine offizielle Zulassung gibt.
Keine Ausnahme: Auch in den Vereinigten Staaten bekamen schwer erkrankte COVID-19-Patienten das Mittel. Mit beeindruckendem Erfolg, glaubt man US-Forschern.
Lesen Sie auch: Alle Entwicklungen rund um das Coronavirus in unserem Live-Blog
Patienten hätten die Klinik binnen einer Woche verlassen
Wie die Gesundheitswebseite "STAT" am Donnerstag berichtete, seien in einem Chicagoer Krankenhaus 125 Patienten, davon 113 schwer erkrankt, täglich mit Remedesivir-Infusionen behandelt worden.
Demnach habe das antivirale Medikament in einer klinischen Studie der University of Chicago Medicine eine rasche Erholung der Erkrankten bei Fieber und Atemwegssymptomen gezeigt. Fast alle Patienten hätten die Klinik binnen einer Woche verlassen können, wie "STAT" erfahren haben will. Zwei Patienten seien gestorben.
Eric Topol, Direktor des medizinischen Scripps Research Translational Institute, bezeichnete die Ergebnisse gegenüber "STAT" als "ermutigend" und als "weiteres positives Signal für die Wirksamkeit des Medikaments".
Die Ergebnisse sind allerdings aus mehreren Gründen mit Vorsicht zu genießen:
- Bisher haben die Forscher die klinischen Daten der Studie oder Teile davon nicht veröffentlicht, sie konnten also bisher nicht von anderen Wissenschaftlern geprüft werden. Die Studie laufe zudem noch.
- Es gab keine Vergleichsgruppe, denen beispielsweise Placebos verabreicht wurden. Das erschwert die Interpretation der Ergebnisse.
- Die University of Chicago Medicine selbst habe laut "STAT" in einer Stellungnahme betont, dass "es verfrüht und wissenschaftlich unsolide sei, zu diesem Zeitpunkt irgendwelche Schlussfolgerungen zu ziehen".
- Nicht zuletzt wurden die Untersuchungen vom Pharmazie- und Biotechnologieunternehmen Gilead in Auftrag gegeben, welches das Mittel selbst herstellt. Gilead hat logischerweise ein Interesse daran, dass das Medikament erfolgreich ist. Nach jetzigem Stand gibt es dafür aber noch keine ausreichenden Wirksamkeitsbelege – was sich durchaus noch ändern kann.
- Gilead selbst betont laut ARD, dass die Daten erst noch analysiert werden müssten, um daraus Schlüsse zu ziehen. Ende April solle es erste Ergebnisse geben.
Laborergebnisse sehen gut aus
Remdesivir richtet sich direkt gegen das Virus und wurde ursprünglich gegen Ebola-Infektionen entwickelt. Da sie damals in der klinischen Prüfung keine guten Ergebnisse brachte, wurde die Entwicklung nicht weiterverfolgt.
Weil erste Laborergebnisse im Einsatz gegen Coronaviren aber gut aussahen, wird Remdesivir unter anderem in Deutschland in zwei klinischen Studien getestet.
An einer internationalen Studie, bei der die Substanz an 600 Patienten mit moderaten Symptomen und an 400 mit schwerer Symptomatik erprobt werden soll, nehmen unter anderem die München Klinik Schwabing, das Hamburger Uniklinikum Eppendorf (UKE) und die Uniklinik Düsseldorf teil.
Sollte die Studie Erfolge bringen, könnte das Mittel bis frühestens Ende 2020 auf den Markt kommen. (afp/dpa/mf)


"So arbeitet die Redaktion" informiert Sie, wann und worüber wir berichten, wie wir mit Fehlern umgehen und woher unsere Inhalte stammen. Bei der Berichterstattung halten wir uns an die Richtlinien der Journalism Trust Initiative.